エンドソームを起点とするシグナル発信機構の解明
 研究代表者
研究代表者
花房 洋
名古屋大学理学研究科生命理学専攻
http://bunshi3.bio.nagoya-u.ac.jp/~bunshi6/matsumoto_japanese/index.html
研究概要
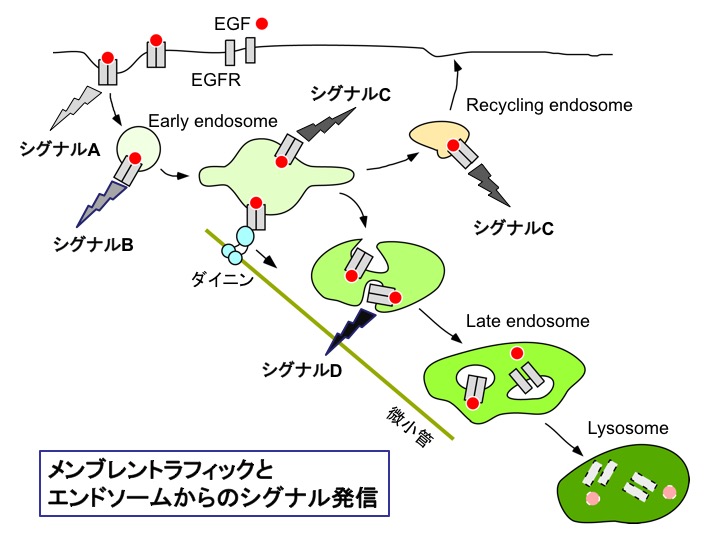
刺激により細胞膜上で活性化した受容体チロシンキナーゼ(RTK)は、エンドサイトーシスによってエンドソームに集積し、リソソームへと運ばれ分解される。この時、受容体の一部は細胞膜にリサイクルされ、リソソームによる分解を免れる。最近の研究から、同じ活性化した受容体が、細胞膜とエンドソームからとで異なるシグナルを発信し、異なった細胞応答を引き起こすことが明らかとなってきた。またエンドソームから発信するシグナルも、エンドソームの成熟に伴って変化することや、リサイクル経路に選別された受容体がシグナルを持続的に発信し続けることもわかってきた。このように同じ受容体から、細胞内の局在場所に依存して異なるシグナル(localシグナル)が発信され、この空間情報こそが細胞応答の特異性決定に重要な可能性が指摘されている。細胞内トラフィックはこれらlocalなシグナル発信を制御している。我々はこれまで、ROCOファミリーキナーゼLRRK1が、上皮成長因子受容体(EGFR)の細胞内輸送を制御し、EGFRシグナルを時空間的に制御していることを明らかにした。LRRK1は活性化したEGFRと複合体を形成し、EGFRのダイニンモータータンパク質依存的な輸送及び、エンドソーム膜上のマイクロドメイン局在に重要な役割を果たしている。このことはLRRK1が、エンドソーム膜マイクロドメインから発信されるEGFRシグナルに関与する可能性を示唆している。そこで本研究では、LRRK1によるRTK細胞内トラフィック制御に注目し、エンドソームを起点としたシグナル発信機構を明らかにしたい。これまでのシグナル研究は、シグナルが“いつ”“どれくらい”活性化しているか測定することが中心であり、“どこで”活性化しているのか空間的な情報(localシグナル)が欠如していた。空間情報を加味したシグナルモデルの構築は細胞応答の特異性を記述するのに重要であり、我々はエンドソームを起点としたlocalシグナルの発信機構に注目し解析することで、数理解析に必要な実測データの取得に貢献できるのではないかと考えている。
参考文献
- Hanafusa, H., Kedashiro, S., Tezuka, M., Funatsu, M., Usami, S., Toyoshima, F., and Matsumoto, K. PLK1-dependent activation of LRRK1 regulates spindle orientation by phosphorylating CDK5RAP2. Nat. Cell Biol.17:1024-1035 (2015)
- Kedashiro, S., Pastuhov, S.I., Nishioka, T., Watanabe, T., Kaibuchi, K., Matsumoto, K., and Hanafusa, H. LRRK1-phosphorylated CLIP-170 regulates EGFR trafficking by recruiting p150Glued to microtubule plus ends. J. Cell Sci., 128:385-396 (2015)
- Ishikawa, K., Nara, A., Matsumoto, K., and Hanafusa, H. EGFR-dependent phosphorylation of Leucine-rich repeat kinase LRRK1 is important for proper endosomal trafficking of EGFR. Mol. Biol. Cell, 23:1294-1306 (2012)
- Hanafusa, H., Ishikawa, K., Kedashiro, S., Iemura, S., Natsume, T., Komada, M., Shibuya, H., Nara, A., Matsumoto, K. Leucine-rich repeat kinase LRRK1 regulates endosomal trafficking of the EGF receptor. Nat. Commun. 2, e158 (2011)








